泰州市食品检验院 江苏泰州 225300
摘要:氟喹诺酮类药物在畜牧、水产等养殖业应用广泛,但由于其给药过程中仅有一部分药物能被生物体吸收转化,并以代谢产物的形式排除体外,大部分的药物则以原型药物的形式经生物体进入自然环境,因此对各类畜、禽产品氟喹酮类抗生素残留量的检测越来越受到监管部门和检测机构的重视。本文将综述氟喹诺酮药物残留的重要检测方法,并阐述我院关于肉类食品中氟喹诺酮类药物残留检测方法的研究进展。
关键词:氟喹诺酮类药物;联用技术;固相萃取
1 氟喹诺酮类药物介绍
氟喹诺酮类药物是上个世纪80年代开发出来的第三代喹诺酮类抗菌药物,代表产品有诺氟沙星(Norfloxacin hydrochloride)、氧氟沙星(Ofloxacin)、环丙沙星(Ciprofloxacin)、恩诺沙星(Enrofloxacin)、盐酸沙拉沙星(Sarafloxacin hydrochloride)、加替沙星(Gatifloxacin)、巴洛沙星(Balofloxacin)等。氟喹诺酮类药物因为其有结构相似、取代位点多、抗菌谱广、药物活性高等特性而受到广泛的应用。上述常见的氟喹诺酮类药物结构式如图1所示,这类药物的作用机理是可直接作用于细菌的细胞核,通过抑制细菌的DNA旋转酶,使旋转酶不能在DNA的双链上引入切口,进而从分子机制上破坏细菌的代谢和增殖,如此既能杀灭细菌也能抑制细菌繁殖。
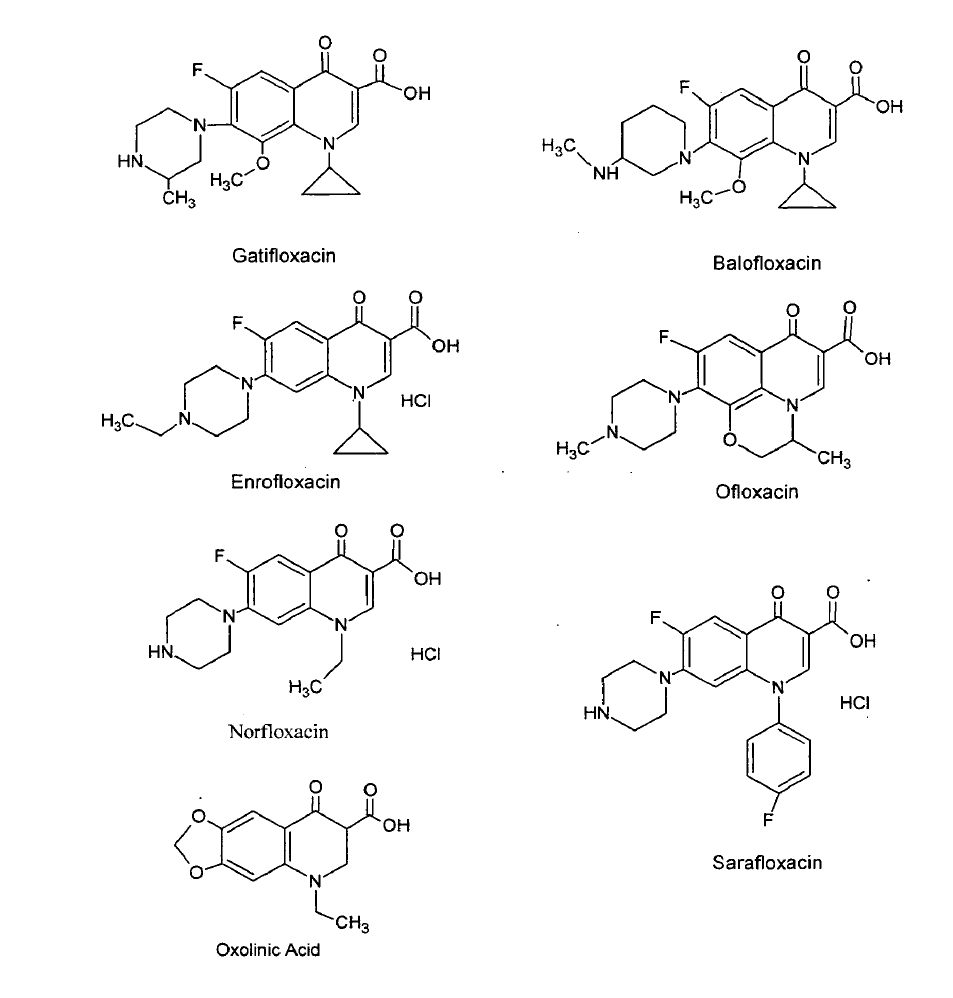
图1 几种常见氟喹诺酮药物的分子式
欧盟自1999年开始对动物的肌肉、肝和肾中氟喹诺酮类兽药残留量规定限值;在中国加入WTO后,对我国出口的动物源性食品中氟喹诺酮类抗生素的残留量实施监测,将检测残留限量控制在0.05mg/kg以内。联合国粮农组织FAO规定氟喹诺酮类抗生素在牛、猪、禽等可食用肌肉组织中的允许残留量为0.2mg/kg。我国虽然对喹诺酮类药物开发应用研究较晚,但目前氟喹诺酮类药物经过药监局批准的已经有十余种,其中主要有诺氟沙星、环丙沙星、氧氟沙星等。当前的国家标准也规定了氟喹诺酮类药物在家禽及生猪的可食部分中的残留限量值为1.9mg/kg。因此,对各类畜、禽产品氟喹酮类抗生素残留量的检测越来越受到监管部门和科研机构的重视。
2 当前主要的检验检测方法及我院的方法研究
作为感染性疾病防治以及抗感染治疗所不可或缺的重要抗生素,氟喹诺酮类药物已在临床上得到了广泛使用,在人类及动物疾病的治疗与预防中发挥着极其重要的作用,因而其品质上的优劣直接关乎着其在实际生产生活中的安全与效用。自抗生素药物问世以来,一直有研究表明,抗生素给药后并不会被动物吸收完全,大部分会随着排泄物被转移到环境中,由此带来环境污染和抗生素残留逐渐提上人类的议事日程。
2.1 微生物方法
抗生素的微生物检测方法是基于量反应平行线的原理,根据合适条件下适量浓度的抗生素可以特异性地抑制甚至杀死某种微生物的特点,以抗生素的抗菌性为标准来评价其有效成分效力的一种方法[1]。微生物检定法是世界上通用的用于测定抗生素的经典方法,是测定抗生素效价(活性)的基本方法。自微生物检定法出现至今,该法已经被陆续收录到了各国的药典中。2010 年版《中国药典》第二部中就收录有93 种抗生素采用微生物检定法进行定量检测[2]。抗生素微生物检定法通常包括比浊法、稀释法以及琼脂扩散法等。H.R.N. Salgado 等采用微生物检定法测定了加替沙星的活性,在 4~16 μg/ml 范围内得到了较好的线性及精确度[3]。该方法能够直观反映抗生素对于微生物的杀菌或者抑菌的能力,但该法耗时长、操作繁、影响因素多、限制条件杂、且检测成本高,并且不能检测无活性的代谢物,尤其是在农产品和食品中药物的残留分析中所起的作用不大,所以应用不多。
2.2 免疫分析法
免疫分析法通常包括两大类,第一类是相对独立的分析方法,如放射性免疫分析(RIA)、酶联免疫法(ELISA)等;第二类是与其他分析技术进行联合使用的方法,如免疫亲和色谱,利用的便是免疫分析的高度选择性结合色谱的有效分析性。目前,酶联免疫法研究较多,这是基于抗原和抗体反应,以酶催化底物作为检测信号的一种免疫分析技术。Zhanhui Wang 等采用竞争性酶联免疫法对鸡肉组织、鸡肝脏、蜂蜜、河虾及鸡蛋样品中的 6 种氟喹诺酮类抗生素进行了加标回收测定,所得总体回收率为 60%~93%,为该法的应用打下了一定的基础。
2.3 核磁共振法
自从核磁共振(nuclear magnetic resonance,NMR)光谱法被发明至今,由于该项技术在分析中需要消耗大量的试样,且灵敏度不高,所以,很长一段时间来该法多用于物质结构的测定,而在定量分析中的应用一直受限。近几十年来,随着科研人员在 NMR 领域中的开创性研究,且仪器装置得到长足的发展,促使 NMR 在检测分析领域逐渐演变为强有力的工具。胡敏等利用 NMR 测定了 9种 FQs 化学对照品的绝对含量,所得结果与标签示值的误差值仅为 1%。目前,NMR定量方法在美国、英国等国的药典中都有收录。但由于药物中所含有的杂质相对很少,所以在杂质检查方面,NMR 还不能对痕量的杂质进行准确的定量。所以在食品中的检测应用还有待进一步的研究。
2.4 色谱质谱联用技术
虽然色谱技术具有很好的分离效果,可以对试样中的组分进行有效的分离,但其在定性、定结构上的能力较为欠缺;在主要成分未知的情况下,通过各组分的保留特性来定性便显得更加困难。随着各类分析手段的不断突破,如质谱、紫外光谱、核磁共振波谱等技术的发展,色谱与上述方法间的联用,使得定性成为了一件较为简单的事情。
液相色谱和质谱联用技术,不仅具有液相色谱对复杂基质食品进行高效分离的能力,而且兼具了质谱的高灵敏度和高选择性,可以准确提供物质相对分子质量以及结构信息,被广泛应用于食品、药品等领域的检测、科研。Haruhiko 等采用 LC-MS 对污水处理厂所排放废水中的氟喹诺酮类药物进行测定,其中氧氟沙星在二级处理水及排污水中的浓度分别为 204 ng/L 和 100 ng/L。Reverte 等采用 HPLC-MS 分析了污水处理厂进出水口处水中的氟喹诺酮类药物残留量,浓缩 1000 倍后所得方法的检出限为 4.0~6.0 ng/L。随着新型质谱技术,如大气压化学电离(APCI)、电喷雾(ESI)等常压化学电离方式的不断发展,极大地拓展了液相色谱-质谱的应用范围,其检测能力广而且灵敏度高,再者其抗基质干扰的能力也很强。饶勇等采用液相色谱-大气压化学电离-离子阱质谱(LC-APCI-ITMSn)联用方法对牛奶中的环丙沙星、诺氟沙星等十种氟喹诺酮类化合物的残留进行了检测分析,所得加标回收率为 60.6%~101.0%,检测限为0.2~0.8 ng/m L。Yang Xiao 等采用 LC-ESI 测定了环境水质中的 20 种喹诺酮类及氟喹诺酮类抗生素,总体回收率为 64%~127%,支流、污水、地表水中的喹诺酮类及氟喹诺酮类抗生素的方法检出限分别为 1.6~50 ng/L,0.6~50 ng/L 和 0.8~50 ng/L。
2.5 基于分子印迹固相萃取技术的色谱质谱联用检测方法
泰州市食品检验院多年来一直开展畜禽肉类农产品、深加工肉制品中抗生素残留量的检测分析研究。20年以来,针对速冻肉制品中氟喹诺酮类抗生素残留的定量分析,我院检测人员研究建立了一套固相萃取-超高效液相色谱-串联质谱的分析方法。
经过前处理后的肉品试样用乙腈(含甲酸)提取后上离心机离心,取上清液使用Oasis PRiME HLB固相萃取柱进行净化,净化液接着采用Acquity UPLC HSS T3色谱柱开始分离,然后以甲酸和甲醇为流动相进行梯度洗脱,分离液在电喷雾(电离正离子)模式下开展测定。经过多次的检测结果表明,该方法在0.1~100μg/L范围内的线性相关系数r2 ≥0.997;方法检出限为0.3μg/kg;方法定量限为1.0 μg/kg。在1.0μg/kg、2.0μg/kg、10.0 μg/kg三个加标水平下该法的回收率在78.7%~106.4%之间,相对标准偏差RSD在 1.26%~11.59%之间。比较上述的其他方法,该固相萃取-色谱质谱联用检测方法具有处理快速、操作简单、灵敏度高、重现性好等特点,适用于冻肉产品中氟喹诺酮类药物的定量检测分析。
3 小结
作为抗感染治疗以及感染性疾病的防治所不可或缺的重要药物,氟喹诺酮类抗生素已在临床上得到了广泛的应用。除了作为人类用药外,在畜牧业、水产养殖业中也有着广泛的应用。但是,随着氟喹诺酮类抗生素的大量广泛使用,其负面效应也在不断的受到人们的关注,如劣质抗生素的不断涌现,畜禽养殖业中的无度无序使用,动物源性食品中抗生素的残留以及人畜抗生素滥用所带来的环境污染等问题,均对氟喹诺酮类抗生素的检验检测方法提出了更高的要求。
随着分析测试技术的不断发展,已有的关于氟喹诺酮类抗生素的分析检测方法的报道虽多,但现有的氟喹诺酮类抗生素分析方法大多存在复杂繁琐的样品预处理过程,样品需求量大,预处理时间长,无法满足高通量分析检测的要求。因此,对于复杂样品中氟喹诺酮类抗生素的检测分析,建立简单、快速、灵敏、准确的检测方法,具有十分重要的意义,今后一段时间内我院还在现有的基于分子印迹固相萃取技术的色谱质谱联用检测方法基础上针对不同品类、不同工艺的动物源性产品中氟喹诺酮类药物的检测方法开展研究。
参考文献
[1]李婷,王玉荣,李成,冯廉洁,陈连剑,江霞.抗生素的分析方法简介,海峡药学,2011,23(6): 78-79.
[2]邵明立.中华人民共和国药典(第二部).北京: 中国医药科技出版社,2010.
[3]李婧.氟喹诺酮类抗生素的直接质谱分析研究[I],东华理工大学,2015,8-9.