1.哈尔滨石油学院,化学工程学院,黑龙江,哈尔滨,150027 2.哈尔滨石油学院,土木工程学院,黑龙江,哈尔滨,150027
摘要:本论文采用液相还原法分别制备Pd/C和Pd-SnO2/C两种催化剂对所制备的催化剂进行XRD测试,并采用循环伏安法和计时电流法对所制备的催化剂对甲酸电催化氧化活性和稳定性进行测试。实验结果显示,Pd-SnO2/C催化剂在对甲酸电催化氧化活性和稳定性都要好于Pd/C催化剂。
关键词:甲酸,Pd基催化剂,电催化活性
能源作为现代社会发展的基础,是实现可持续发展的前提条件。当前,人类社会对能源的需求主要依赖化石燃料,如石油、煤和天然气等。然而,随着全球人口的增长以及城市化的进程,对能源的需求量呈现出持续上升的趋势。因此,能源问题与环境污染问题已成为21世纪的两大关注焦点。人们开始认识到发掘和推广绿色、清洁、可持续能源的重要性[1-3]。因此,寻求绿色新能源以缓解能源危机和环境污染已成为本世纪关注的核心议题之一。现阶段,可持续新能源的研究领域主要涵盖太阳能、风能、地热能以及燃料电池。特别是燃料电池,作为一种高效、环保的绿色新能源,引发了全球的广泛关注[4-7]。
近些年科研人员来通过不断的研究发现,直接甲酸燃料电池(DFAFCs)与直接甲醇燃料(DMFCs)电池相比有着明显的优势[8]。甲酸具备诸多优势,成为研究热点。例如,与甲醇相比,甲酸没有毒性、且不易燃,更方便储存和运输。其理论开路电位可达1.45V,且对Pt基电催化剂的毒化较低,这些特点皆为其应用提供了方便。
文献上广泛被科研人员接受的甲酸氧化机理是通过平行反应进行的:(1)在“直接途径”中直接生成CO2,没有任何中间产物;(2)在“间接途径”中,甲酸有中间产物CO产生,然后被氧化最终生成CO2。经研究发现,甲酸在Pd催化剂上主要是通过直接途径氧化,因此Pd是一种很好的甲酸电催化氧化的催化剂[10]。
近些年来科研人员发现,Pd/C催化剂虽然广泛应用于甲酸燃料电池的应用,但同时也存在一些的明显的不足[11,12]:(1)在甲酸氧化的过程中,Pd/C催化剂的稳定性和耐受性不够理想。由于其容易受损的特性,氧化电流可能会出现急剧下降的情况。(2)在酸性电解质中,碳载体在高电位下长期实验时,很容易被腐蚀。因此,对于实现甲酸燃料电池商业化,研究和设计具有高催化活性和稳定性的Pd基电催化剂至关重要。
研究发现,在Pd/C催化剂中加入第二种物质,形成二元Pd基催化剂的效果很好,为此很多科研人员做了大量的研究。截至目前,报道的Pd合金化金属Ru、Zn、Sn、Ni、Co、Ir等[13],均说明Pd与其他金属的合金化可以降低Pd的成本,提高催化剂的稳定性,同时具有较好的催化性能;因此,吸引了众多研究者的青睐。
本实验是在碳载体中引入SnO2,形成Pd-SnO2/C催化剂,通过研究电化学测试研究SnO2对Pd/C电催化活性的影响。
1.实验部分
1.1仪器和试剂
活性炭(美国E-TEK公司产品,型号Vulcan XC-72),数控超声波清洗器(昆山市超声仪器有限公司,型号KQ2200DB),氮气为纯度为高纯氮气(哈尔滨黎明气体有限公司,纯度为99.99%),电化学分析仪(上海辰光仪器公司,型号CHI-650)和常规的三电极电化学电池进行电化学测试。实验过程中,所使用试剂规格均为分析纯,所用的水均为二次蒸馏水。
1.2催化剂及电极的制备
1.2.1 Pd/C催化剂的制备
将0.2g活性炭与10mL乙二醇混合超声振荡1.5小时后,再加入10mL乙二醇,回流加热至80oC然后搅拌2小时,然后80oC在加入PdCl2溶液21mL(溶液浓度为4g/L,溶液中Pd的质量分数为59.5%);用2molL-1NaOH调节pH﹦12。向上述溶液滴加HCOOH溶液在搅拌中还原2小时。然后搅拌中降至室温。抽滤、洗涤至无Cl-存在,用二次蒸馏水抽滤、洗涤至无Cl-存在,随后在80oC时,真空干燥10小时,得到Pd质量份数为20%的Pd/C催化剂。
将分析纯SnO2与碳载体混合,在室温条件下,超声分散2h后,通过磁力搅拌器搅拌8h,合成SnO2/C载体。然后,在采用上述方法制备Pd-SnO2/C催化剂。根据相关计算,制备的催化剂中Pd-Sn的摩尔比为2:1。
1.2.2 电极的制备
分别取所制备的两种催化剂2.5mg,放入到小烧杯中。然后依次向小烧杯中加入全氟磺酸树脂溶液(Nafion)11.5μL,聚四氟乙烯乳液(PTFE)10μL及少量乙醇,充分混合后,再采用超声振荡。大约振荡5min后,小烧杯中出现类似“油墨”状混合液,将此混合液均匀的涂在碳纸上,在室温下进行干燥,即可得到Pd/C电极。所得到的催化剂电极表面积为0.5cm
2,其中Pd的负载量为1mg·cm2,PTFE含量约为25%,Nafion含量约为13%.
1.3 电化学测量
电化学测量所采用的是常见三电极系统,其中自制的催化剂电极作为工作电极,铂电极作为辅助电极,银-氯化银(Ag-AgCl)电极作为参比电极。在进行电化学测量之前,为了更好的进行电化学测试结果,先将电解池及溶液中的氧气除去,具体操作为向电解池中通入一定量的高纯氮,实验是在25±1oC温度下进行的。
XRD分析的目的是用于测试催化剂的结晶度、粒径大小以及催化剂的晶面。
所采用的仪器设备是日本理学转靶X射线衍射仪(型号D/max-3B),Cu Kα靶,管电压为40Kev,管电流为30mA。
2.结果与讨论
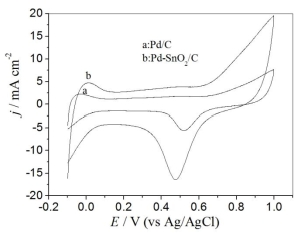
图1 Pd/C和Pd-SnO2/C催化剂
在1.0mol·L-1H2SO4溶液中循环伏安曲线
图1是两种催化剂在指定燃料(1.0mol·L-1 H2SO4)中进行的溶液中的循环伏安曲线。可以明显从图中观察到,Pd-SnO2/C催化剂的电化学比表面积要大于Pd/C催化剂。
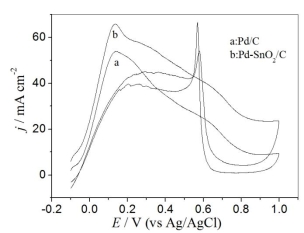
图2 Pd/C和Pd-SnO2/C催化剂
在1.0mol·L-1HCOOH+1.0mol·L-1H2SO4溶液中循环伏安曲线
图2是两种催化剂在指定燃料(1.0mol·L-1HCOOH+1.0mol·L-1H2SO4)溶液中的循环伏安曲线。由图观察可以,在Pd/C和Pd-SnO2/C催化剂电极上甲酸正扫方向氧化峰的电流密度分别是54.0mAcm-2和66.05mAcm-2,两种催化剂的峰电位相同均为0.136V。从氧化峰的电流密度来看,Pd-SnO2/C催化剂的氧化峰电流密度是Pd/C催化剂的1.22倍。这说明Pd-SnO2/C对甲酸电催化氧化性能要好于Pd/C。
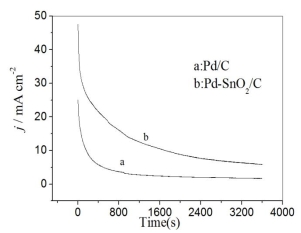
图3 Pd/C和Pd-SnO2/C催化剂
在1.0mol·L-1HCOOH 1mol·L-1 H2SO4)溶液中的计时电流曲线
图3是两种催化剂电极指定燃料(1.0mol·L-1HCOOH 1mol·L-1 H2SO4)溶液中,在0.06V时的计时电流曲线。由图可见,该时间测试为1h,在测试结束时,Pd/C的电流密度分别为1.91mAcm-2,而Pd-SnO2/C催化剂电极上的电流密度为5.88mAcm-2,可以的看出Pd-SnO2/C催化剂的电流密度明显好于Pd/C催化剂,说明Pd-SnO2/C催化剂对甲酸电催化氧化的稳定性要强于Pd/C催化剂。进而说明,Pd-SnO2/C对甲酸电催化氧化性能要好于Pd/C。
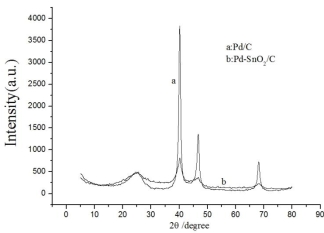
图4 Pd/C和Pd-SnO2/C催化剂的XRD图形
图4是两种催化剂的XRD图形。通过图片可以明显发现,除了炭的特征峰在24.95之外,2还对应其他三个角度的峰值分别是40.28,46.66和68.28。这三个峰值所对应分别是面心立方结构的Pd晶体的Pd(111),Pd (200)和Pd(220)。由于Pd(220)衍射峰基本上不与活性炭(002)晶面的衍射峰重叠,所以通常用于这一衍射峰计算Pd粒子的平均粒径。在Pd-SnO2/C催化剂中Pd(220)的峰值要比Pd/C催化剂中Pd(220)的峰值稍宽,说明Pd粒子在Pd-SnO2/C催化剂中的粒子要小于Pd/C催化剂中的Pd粒子,从而使Pd粒子在Pd/C催化剂中有较大的比表面积。
3结论
通过对所制备催化剂进行性能相关的电化学性能测试,发现Pd-SnO2/C催化剂在对甲酸催化氧化的性能方面要优于Pd/C催化,这可能是由于SnO2的加入,增加了催化剂的稳定性。此外,由于SnO2的加入,在提供大量的OHads时,会更加容易除去COads,从而达可以将甲酸氧化的中间产物快速移除反应系统,进而使催化剂活性增强。
参考文献
[1]Huang H, Wang X. Recent progress on carbon-based support materials for electrocatalysts of direct methanol fuel cells. Journal of Materials Chemistry A, 2014, 2(18): 6266-6291
[2]Islam M T, Shahir S A, Uddin T M I, et al. Current energy scenario and future prospect of renewable energy in Bangladesh. Renewable & Sustainable Energy Reviews, 2014, 39(6): 1074-1088
[3]Nie Y, Li L, Wei Z. Recent advancements in Pt and Pt-free catalysts for oxygen reduction reaction. Chemical Society Reviews, 2015, 44(8): 2168-2201
[4]Steele B C, Heinzel A. Materials for fuel-cell technologies. Nature, 2001, 414(6861): 345-352
[5]Debe M K. Electrocatalyst approaches and challenges for automotive fuel cells. Nature, 2012, 486(7401): 43-51
[6]Wang S, Jiang S P. Prospects of fuel cell technologies. National Science Review, 2017, 4(2): 163-166
[7]Wang Y, Tao L, Xiao Z, et al. 3D Carbon electrocatalysts in situ constructed by defect-rich nanosheets and polyhedrons from nacl-sealed zeolitic imidazolate frameworks. Advanced Functional Materials, 2018, 28(11): 1705356-1705362
[8]裴昱昊. 直接甲酸燃料电池阳极Pd基催化剂复合载体性能的研究. 哈尔滨师 范大学,2022
[9]吴密密. 直接甲酸燃料电池阳极Pd基多元复合催化剂的研究. 湖南大学, 2018
[10]梅正繁. 甲酸燃料电池阳极Pd基碳化物载体与合金催化剂研究.哈尔滨工业大学,2020
[11]Jung W S, Han J, Ha S. Analysis of palladium-based anode electrode using electrochemical impedance spectra in direct formic acid fuel cells. Journal of Power Sources, 2007, 173(1): 53-59
[12]Geraldes A N, Silva D F D, Silva J C M D, etal. Palladium and palladium-tin supported on multi wall carbon nanotubes or carbon for alkaline direct ethanol fuel cell. Journal of Power Sources, 2015, 275(275): 189-199
[13]陈少峰,侯兰凤,廖世军.钯基催化剂应用于甲酸电氧化反应的研究进展[J].无 机盐工业, 2021, 53(5):33-38+65
项目来源:2023年度黑龙江省大学生创新创业训练计划项目(S202313299051)
通讯作者:许伟锋,(1978-),男,副教授,
哈尔滨石油学院,化工实验中心主任,
研究方向:直接甲酸燃料电池阳极催化剂
![]()